Orbitální pasti ve vývoji vakcín a biofarmak
26. 3. 2021
Biofarmaka zaujímají vedle kompletně synteticky připravených látek významnou a stále expandující oblast na poli léčiv. Může se jednat o krev a krevní komponenty, buňky, tkáně, vakcíny či celé živé organismy, ale hlavně monoklonální protilátky (mAb, struktura proteinu) a fúzní proteiny, které na trhu podle serveru Pharmacompass.com dominují. Díky nim se poslední léta biofarmaka umísťují v žebříčcích nejprodávanějších (dle objemu peněz) léčiv na předních příčkách a v loňském roce se jich v prvních deseti umístilo úctyhodných šest (viz Obr. 1). Biologická léčba (tedy taková, kde jsou použita biofarmaka) našla nezastupitelnou roli ve zvyšování kvality života při onkologické a imunologické terapii nejen díky své efektivitě, ale hlavně díky minimalizaci vedlejších účinků. Použití monoklonálních protilátek nabralo další mimořádný rozmach v současném pandemickém období po objevu casirivimabu a imdevimabu (Regeneron) či bamlanivimabu (AbCellera Biologics/Eli Lilly), po jejichž aplikaci se pacientům nerozvine těžší forma onemocnění.
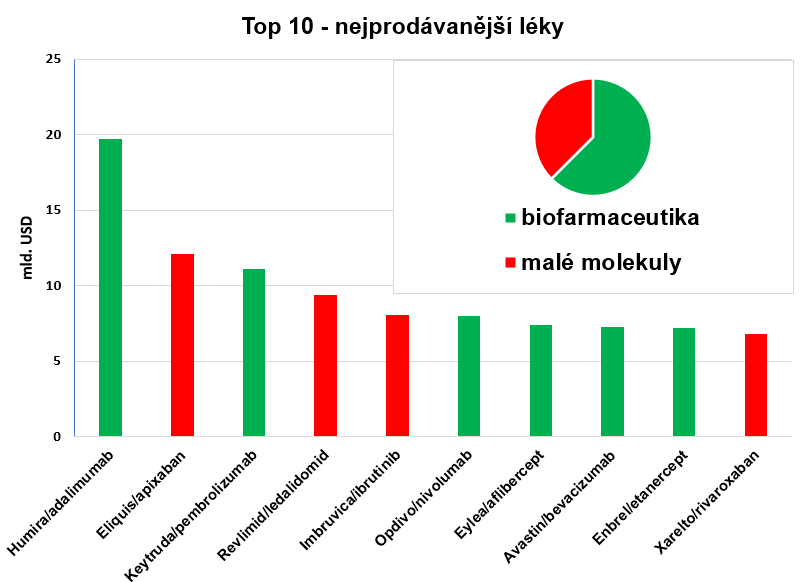
Obr. 1: nejprodávanější léčiva/účinné látky dle serveru pharmacompass.com
Vakcíny nikdy nepatřily k hlavním tahounům farmaceutického průmyslu, což se však může brzy změnit díky současnému koronavirovému rozšíření (milovníci konspiračních teorií zvedají obočí). Nelze opomenout fakt, že významní potenciální producenti očkovacích agens proti SARS-CoV-2 viru nekonstruují vakcínu na bázi oslabených či mrtvých virů jak je běžně zvykem (např. Sinopharm), ale na základě produkce in vitro v bioreaktorech (Novavax, Moderna, Pfizer) nebo in vivo v těle po vakcinaci (Astra Zeneca, Johnson&Johnson, Sputnik V) tzv. spike proteinů („satelitní struktury“ na povrchu viru, viz Obr. 2), které mají přítomnost koronaviru navodit a nastartovat kýženou imunitní reakci.
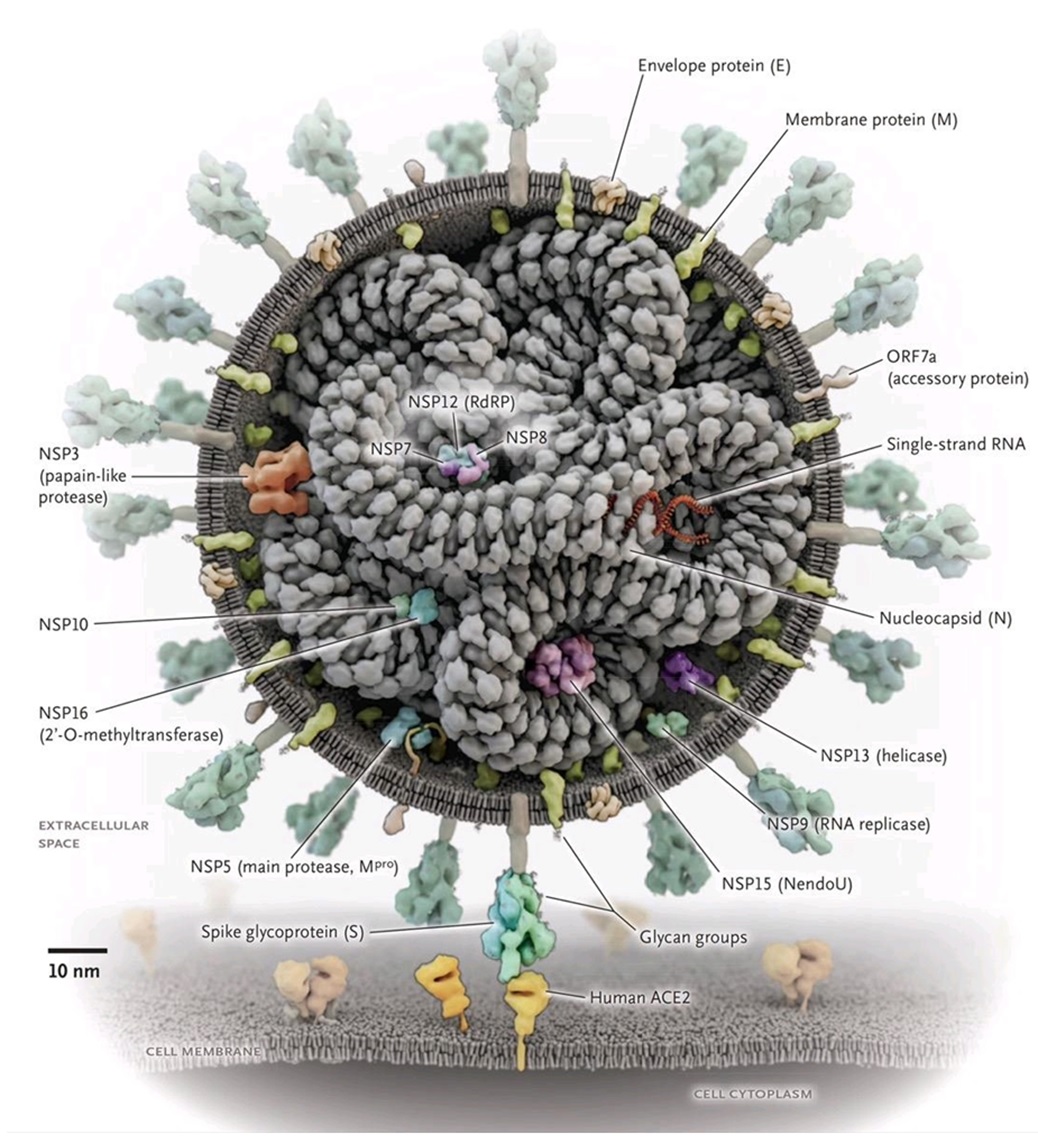
Obr. 2: skladba SARS-CoV-2 viru spolu s proteinovými strukturami (N Engl J Med 2020; 382:2261-2264)
V kontextu s výše uvedenými skutečnostmi stojí analytičtí chemici před úkolem, jak zvládnout charakterizaci a následnou kvantifikaci účinných látek a potenciálních nečistot. Specialisté přicházející z prostředí ortodoxních molekulárně biologických technik nastavili a formálně v direktivách ukotvili praktická a v jistých mezích i dostatečná kritéria s pomocí technik jako je ELISA a SDS-PAGE. Jiní specialisté (léta bičovaní regulemi jakosti syntetických molekul), kteří využívají moderní chromatografické postupy s vysoko rozlišující hmotnostní spektrometrií (HRMS) bývají často zaskočeni, udiveni a navrhují nekompromisní zásahy založené na masivním využití platformy HRMS. Vždyť i k biologickým léčivům lze přistupovat v komplexním analytickém pojetí (i nejprodávanější účinnou bio-látku adalimumab lze popsat sumárním vzorcem C6428H 9912N1694O1987S46).
První logický krok s HRMS přístupem se nabízí provést chromatografickou separaci na reverzní fázi s následnou hmotnostně spektrometrickou analýzou. Zde platí pravidlo o nastavení co největšího rozlišení na hmotnostním spektrometru (běžně 150 000, nejlépe > 200 000 FWHM), čemuž vyhovují spektrometry s iontovou cyklotronou rezonancí nebo orbitální pastí. Díky cenové dostupnosti, bench-top uspořádání a nízkým provozním nákladům se orbitrapy (viz Obr. 3) stávají první volbou. Krásně vykreslená obálka různých nábojových stavů monoklonální protilátky ve stavu denaturovaném a nativním je znázorněna na Obr 4. Zajímavé zjištění přinese zoom jednoho nábojového klastru, resp. spektrum po dekonvoluci, kde lze elegantně pozorovat glykosylační adukty (lišící se počtem navázaných galaktózových jednotek, tj. s hmotnostním rozdílem 162), produkty posttranslační modifikace při bioprodukci. Detailní studium glykosylace může být provedeno iontově chromatografickou separací po kyselé hydrolýze (analýza monosacharidů)) nebo po glykosidázovém štěpení (analýza glykanů/oligosacharidů) nebo proteomickým bottom-up přístupem.
Další krok při charakterizaci biofarmak by měl směřovat k ortogonální separaci (proti reverzní fázi) na iontoměniči. Protože monoklonální protilátky a fúzní proteiny mají díky přítomnosti amino- a karboxylových skupin dostatečný náboj v širokém rozmezí pH, očekává se zajímavý profil, neboť na základě poznatků z glykosylačních studií podléhají biofarmaka rozsáhlým posttranslačním modifikacím. Výsledek je bez zardění překvapující. Díky vazbě až dvou molekul lysinu na C-konce protilátky a procesu vícenásobné deamidace aminokyselin asparaginu a glutaminu v řetězci proteinu dochází k tvorbě (a nikoliv na úrovni stopových množství) k řadě různě nabitých variant oddělitelných jak chromatograficky tak i hmotnostně spektrometricky, viz Obr. 6, 7 a 8.
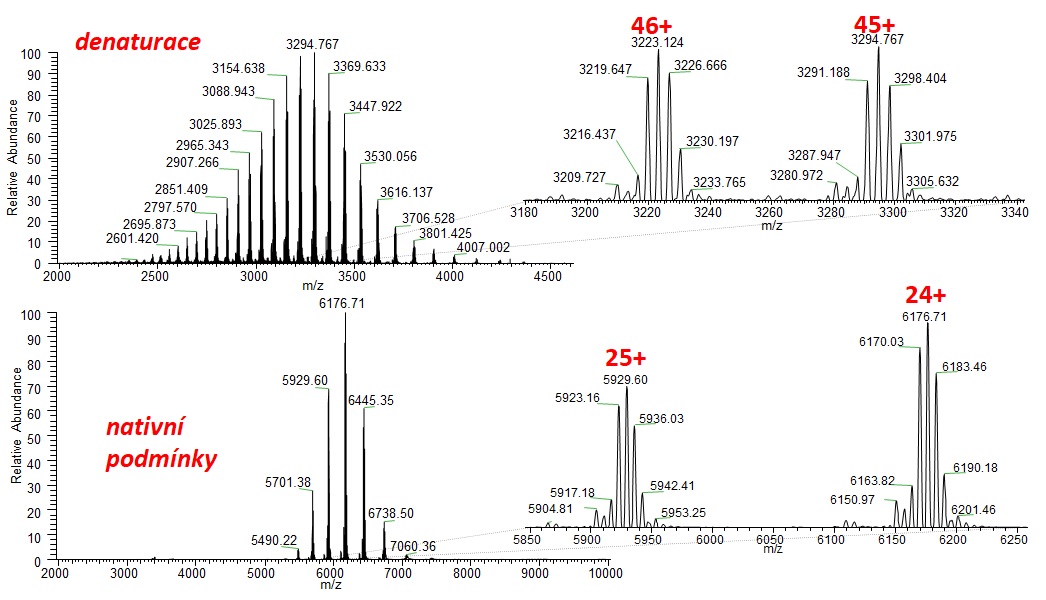
Obr. 3: hmotnostní spektrum adalimumabu, ESI+, rozlišení 200 000 FWHM, orbitální past
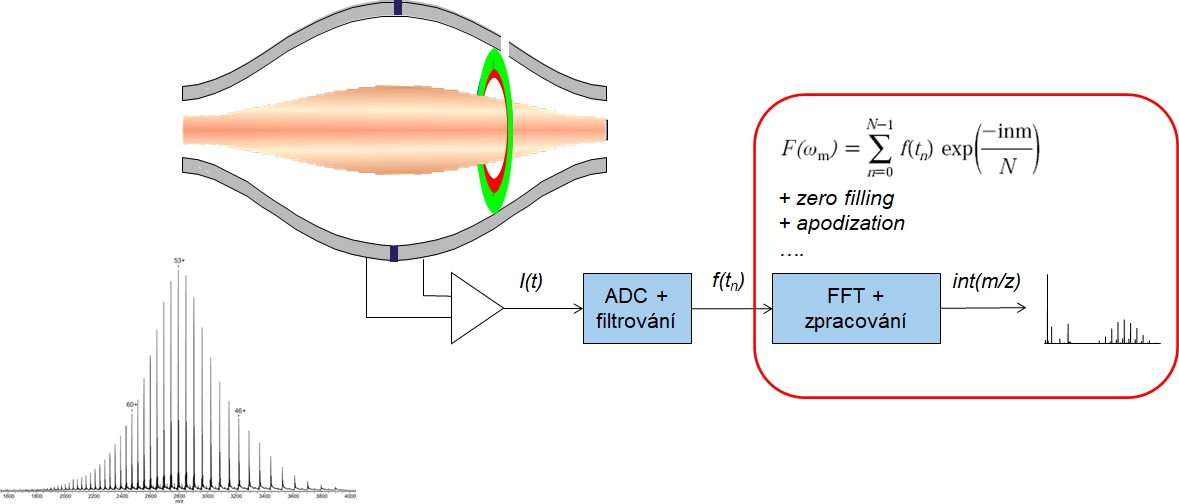
Obr. 4: princip detekce a zpracování signálu na orbitální iontové pasti
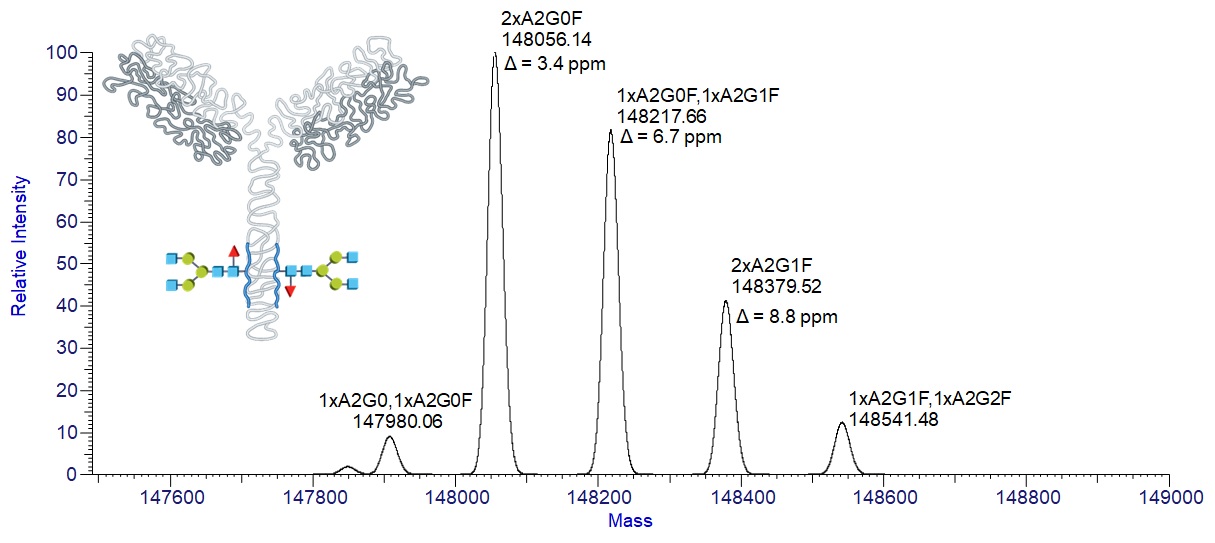
Obr. 5: glykosylační adukty adalimumabu (lišící se počtem navázaných galaktózových jednotek, tj. s hmotnostním rozdílem 162), produkty posttranslační modifikace při bioprodukci
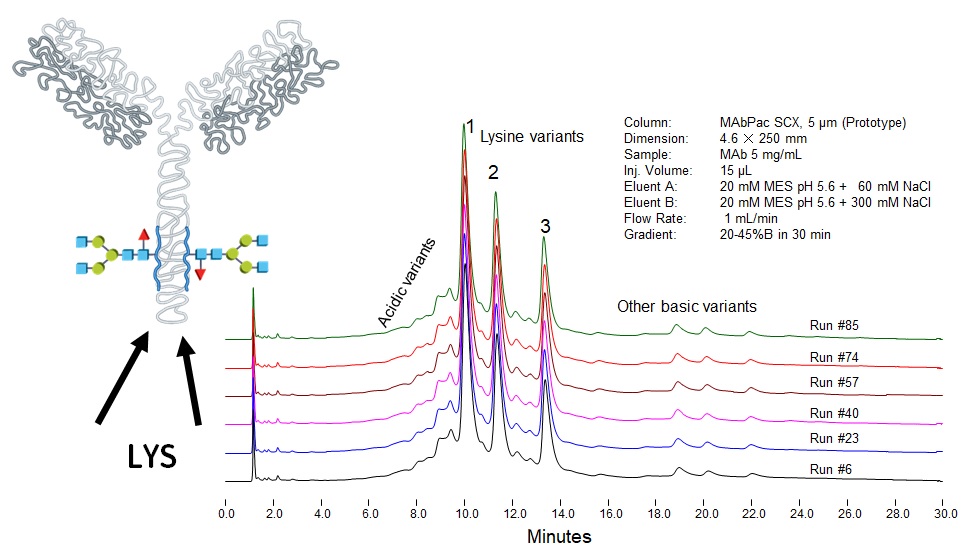
Obr. 6: chromatografická separace finální monoklonální protilátky na iontoměniči odhalující přítomnost nábojových variant
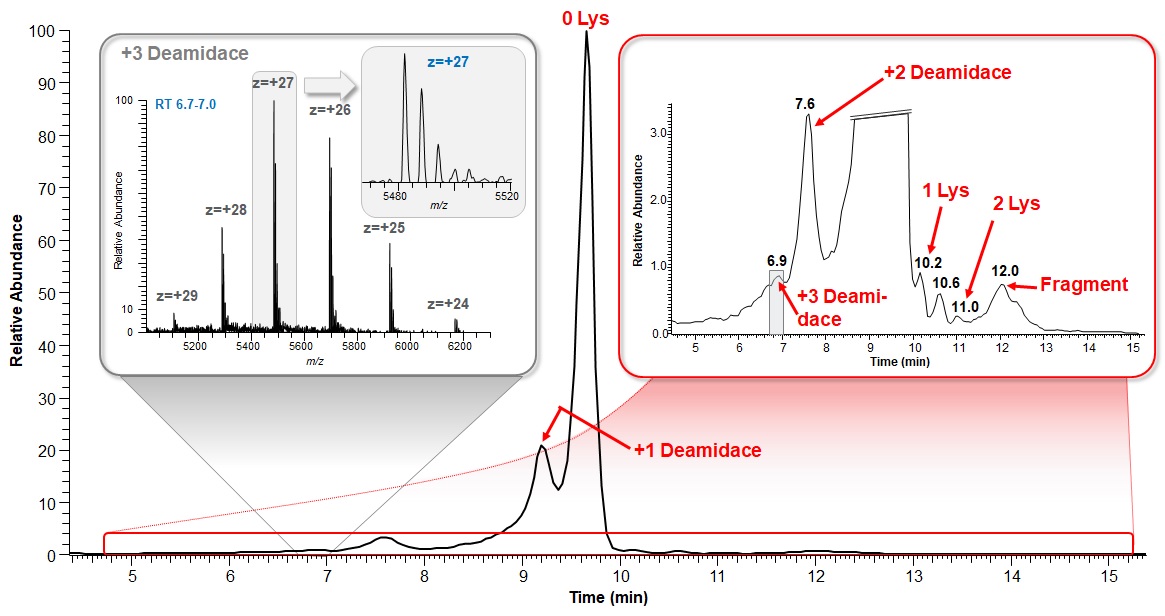
Obr. 7: chromatografická separace adalimumabu na iontoměniči odhalující přítomnost nábojových variant (deamidace + lysinové modifikanty); HRMS spektrum dokladuje charakterizaci trojnásobného deamidačního produktu, navíc glykosylovaného, na nízké koncentrační úrovni
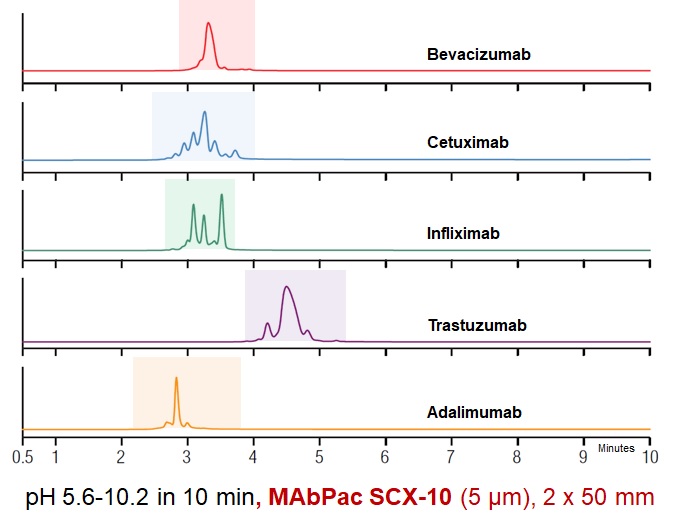
Obr. 8: profily jednotlivých finálních forem komerčně dostupných biofarmak z pohledu přítomnosti nábojových variant z procesu posttranslační modifikace
Studium dalších a dalších modifikací biofarmak se zdá být bezbřehé. S orbitálními pastmi lze odhalovat oxidace na methioninu a tryptofanu, tvorbu pyroglutamátů nebo např. rozpad disulfidické vazby; významná kapitola odhalování nečistot při bioprocesu je také detekce a následná eliminace proteinů z hostitelské buňky (host cell proteins). Podpora a implementace moderních chromatografických a hmotnostně spektrometrických postupů se stává klíčem k úspěšnému analytickému zvládnutí problematiky charakterizace a kvantifikace biofarmak a příbuzných nečistot a není bez zajímavosti, že všechny přední společnosti zabývající se vývojem a výrobou vakcín a monoklonálních protilátek jsou vybaveni hmotnostními spektrometry na bázi orbitrapů s velmi vysokým rozlišením.
Nenechte si ujít další zajímavosti
- Stanovení fluoru v textiliích pomocí spalovací iontové chromatografie (CIC) podle ISO/NP 20999:2023
- Záhada neviditelného dusíku: Proč lehčí neznamená vždy lépe průchodné?
- Hypulse Surface Analysis System
- Vanquish Access – dostupné řešení spolehlivých HPLC analýz
- Psychoreologie a tribo-reologická charakterizace pudinků ve vztahu k textuře